膵癌(すい臓がん)に期待される最新の治療法5つをまとめて紹介

膵癌(すい臓がん)は年々増加傾向にあり、日本におけるがん死亡者数の第4位を占めるまでになっています。
膵臓がんの特徴は、なんと言っても「治療がむずかしい(難治性)」の一言につきます。
実際に、膵臓がんの5年生存率は消化器のがんのなかで最も低く、依然として10%以下です。
これは、診断がついた時にはがんがまわりの臓器や血管へ広がっていたり、すでに遠くの臓器に転移したりしている患者さんが多く、手術(切除)ができないことが最大の原因と考えられています。
一方で、膵臓がんに対して新たな治療法が開発・導入されています。
とくに、最近では個々のがんの遺伝子異常や表現系(フェノタイプ)に応じた個別化治療(オーダーメード治療、プレシジョンメディシン)の波が膵臓がんにも押し寄せています。
今回は、この予後の悪い膵臓がんに対して期待される治療法(すでに承認されたものや臨床試験中のものを含む)を5つ紹介します。
膵臓がんに対して期待される治療法5つ
術前補助化学療法(ゲムシタビン+S1)
これまでは、切除ができる膵臓がんに対しては、すぐに手術を行っていました。
しかし、切除はできたものの組織の端っこにがんが残っていたり、術後早期に再発することが問題でした。
最近、切除可能な膵臓がんや、重要な血管に接していて切除ができるかどうか微妙な膵臓がん(ボーダーライン膵癌といいます)に対する術前の抗がん剤治療(術前補助化学療法またはネオアジュバント療法ともいいます)の有効性が報告されるようになってきました。
これは、手術の前に一定期間抗がん剤治療を行い、その後、手術を行うものです。
術前抗がん剤治療の予想されるメリットとして、がんの広がりが狭くなることで、がんが残らずに完全切除(いわゆる治癒切除)できるケースが増えること。
あるいは、切除がきびしい膵臓がん(ボーダーライン膵癌)の場合、抗がん剤が効いてがんが小さくなったり、また重要な血管から離れれば、切除可能な状態となることが考えられています。
日本では、ゲムシタビン(ジェムザール)とS-1(ティーエスワン)という2つの薬を併用したGS(ジーエス)療法による術前補助化学療法の安全性と有効性を調査するランダム化比較試験(Prep-02/JSAP-05試験)が行われ、その結果が2019年1月に開催された海外での学会(ASCO-GI 2019)にて報告されました。
この試験では、切除可能な膵臓がんの患者さんを、試験群(術前にGS療法を2コース行い、その後切除)と対照群(いきなり切除)の2つのグループにランダムに割り付けました(どちらの群も術後はS-1による補助化学療法を追加)。
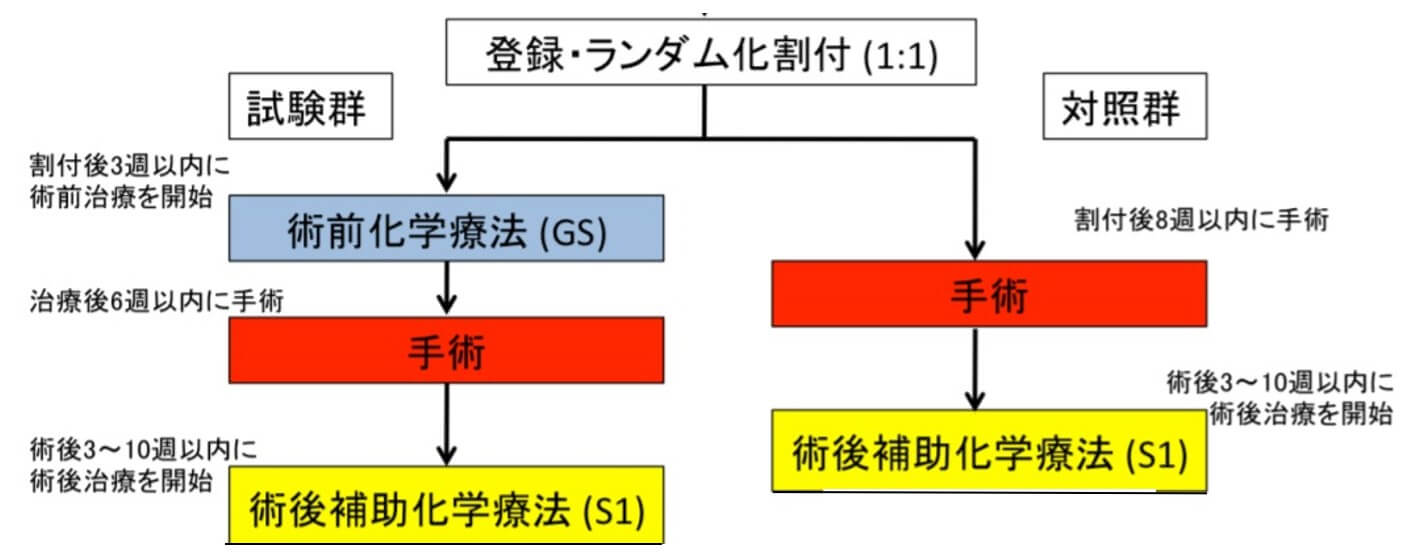
その結果、試験群(術前化学療法+手術)では、対照群(手術先行)と比べてリンパ節転移が少なく、また術後の肝転移再発が少ないという結果に加え、有意に生存期間が延長していました(下図)。
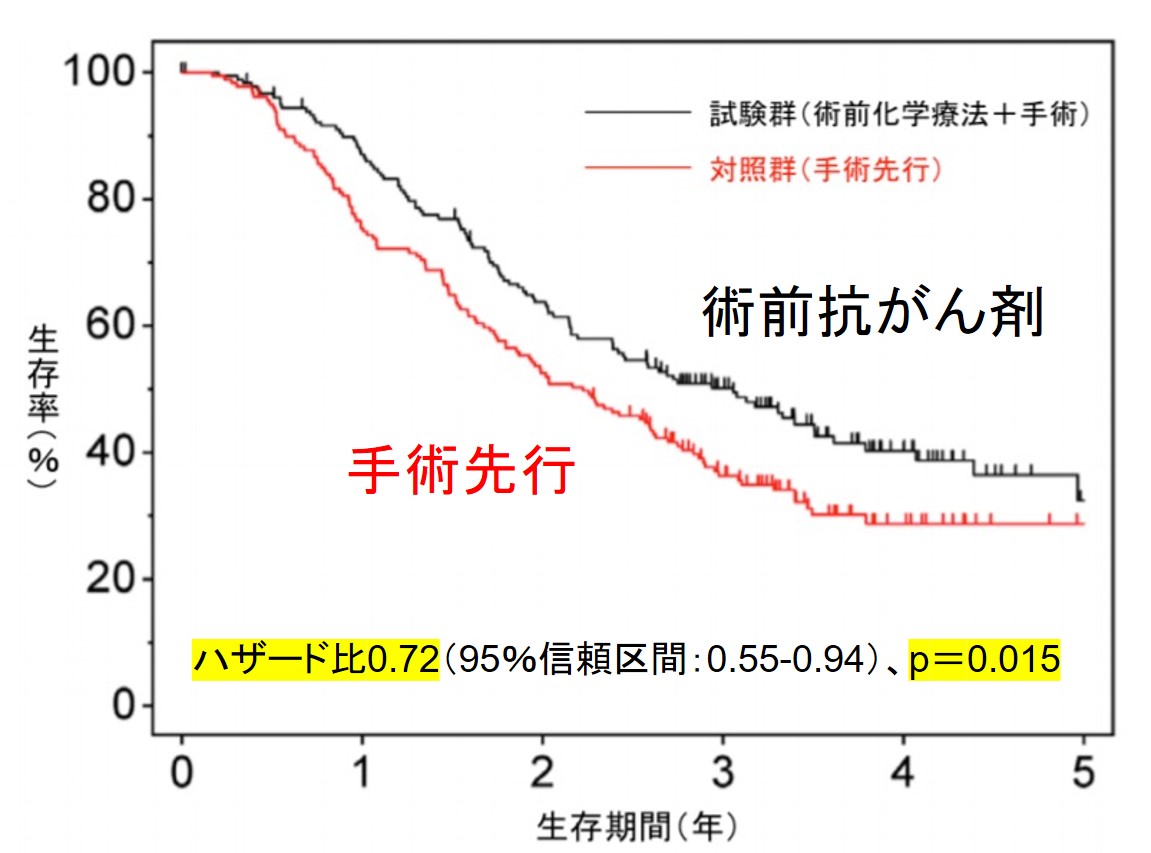
このほかにも、FOLFIRINOX療法やゲムシタビン+ナブパクリタキセル療法などによる術前補助化学療法も期待されています。
今後、ガイドラインにおいても術前補助化学療法が標準治療として加わる可能性が高いと考えられます。
国内での状況:ゲムシタビンもS-1も膵臓がんに承認されている治療薬ですが、術前に使用することは保険適用となっていません。現時点では、切除可能膵臓がんに対する術前補助化学療法は臨床試験として行われている段階です。
キイトルーダ(ペンブロリズマブ)抗PD-1抗体
メラノーマや肺がんなどに画期的な効果をもたらした免疫チェックポイント阻害剤である抗PD-1抗体「キイトルーダ(ペンブロリズマブ)」ですが、2018年12月からは、一部の膵臓がん(ある遺伝子異常のタイプを示す全ての固形がん)にも使用可能となりました。
正確には、「がん化学療法後に増悪した進行・再発の高頻度マイクロサテライト不安定性(MSI-High)を有する固形癌(標準的な治療が困難な場合に限る)」への適応拡大です。
これは、遺伝子修復機能が欠損した特殊なタイプのがんのことで、「MSI検査キット(FALCO)」によってMSI-Highであれば、膵臓がん患者さんにもキイトルーダを使えるようになりました。
具体的には、5種類のMSIマーカー(BAT‑26、NR‑21、BAT‑25、MONO‑27、NR‑24)の中で、MSI+と識別されたMSIマーカーの数により、以下の判定基準に従ってMSI検査の結果を判定し、キイトルーダ適応の可否を判断します。

ただ、膵臓がんではMSI-Highの頻度はとても少なく(3%以下)、実際には対象となる患者さんはごく一部に限られると考えられています。
国内での状況:標準的な治療(抗がん剤)が困難な進行・再発した膵臓がんのうち、検査によってMSI-Highであれば保険適応でキイトルーダを使用できます。ただし、まだ膵臓がんに対しての治療は始まったばかりで、実際の効果や安全性についての評価は定まっていません。
腹膜播種に対する「S-1+パクリタキセル経静脈・腹腔内投与併用療法」
膵臓がんの転移にはいろいろなパターンがありますが、なかでもがん細胞が腹腔内(ふくくうない)へ広がる腹膜転移(あるいは腹膜播種:ふくまくはしゅ)は最も厄介です。
腹膜転移に対しては抗がん剤治療がなかなか効かないことや、腸閉塞や腹水など様々な合併症を引き起こすことが問題となっています。
この膵臓がんの腹膜播種に対して、関西医科大学外科の里井壯平先生らが中心となり、「S-1+パクリタキセル経静脈・腹腔内投与併用療法」の効果について研究を行っています。
この治療は、すでに膵臓がんで標準的に使われている経口抗がん剤である「S-1」と、胃がんや乳がんなどに優れた治療効果がある「パクリタキセル」を点滴剤として併用し、さらに「パクリタキセル」をおなかの中に投与する治療方法により腹膜転移に対してがんの進行を制御することがその目的です。
日本の多施設による第2相臨床試験の結果はすでに報告されており、以前のブログ記事で紹介しました。
治療のおもな結果は以下のとおりでした。
■ 全患者の生存期間の中央値は16.3ヶ月(11.5~22.6ヶ月)であり、1年生存率は62%、2年生存率は23%でした。
■ 客観的奏功率(がんが30%以上小さくなった部分寛解の割合)は36%であった。
■ 病勢コントロール率(がんの進行がなかった割合)は82%であった。
■ 15人中9人(60%)で治療開始から1年以内に腹水が消失した。
■ 抗がん剤投与によって切除可能となり、膵切除術を行った8人では、手術を受けなかった患者に比べて有意に生存期間が長かった(手術を受けた患者の生存期間の中央値は27.8ヶ月)。
以上の結果より、腹膜転移を認める膵臓がん患者に対して有望な治療法であるとしています。
現在、第3相試験の実施にむけてクラウドファンディングで資金提供を募っています。
この第3相試験の結果によっては、将来的に膵臓がんの腹膜播種に対する治療法として承認される可能性が高いと思います。
国内での状況:保険未承認の治療法です。上記のように第3相臨床試験が準備中。
BRCA変異陽性の膵臓がんに対するオラパリブ(PARP阻害剤)
オラパリブは、DNAの修復酵素であるPARP(ポリADP-リボースポリメラーゼ)を阻害する分子標的薬の1つです。
最近、BRCA遺伝子変異が陽性の転移性膵臓がん患者(ステージ4)に対するオラパリブの効果を調べたランダム化比較試験の結果が報告され、オラパリブは無増悪生存期間(progression free survival)を有意に延長し、進行(または死亡)のリスクをおよそ半分も減らすことが確認されました。
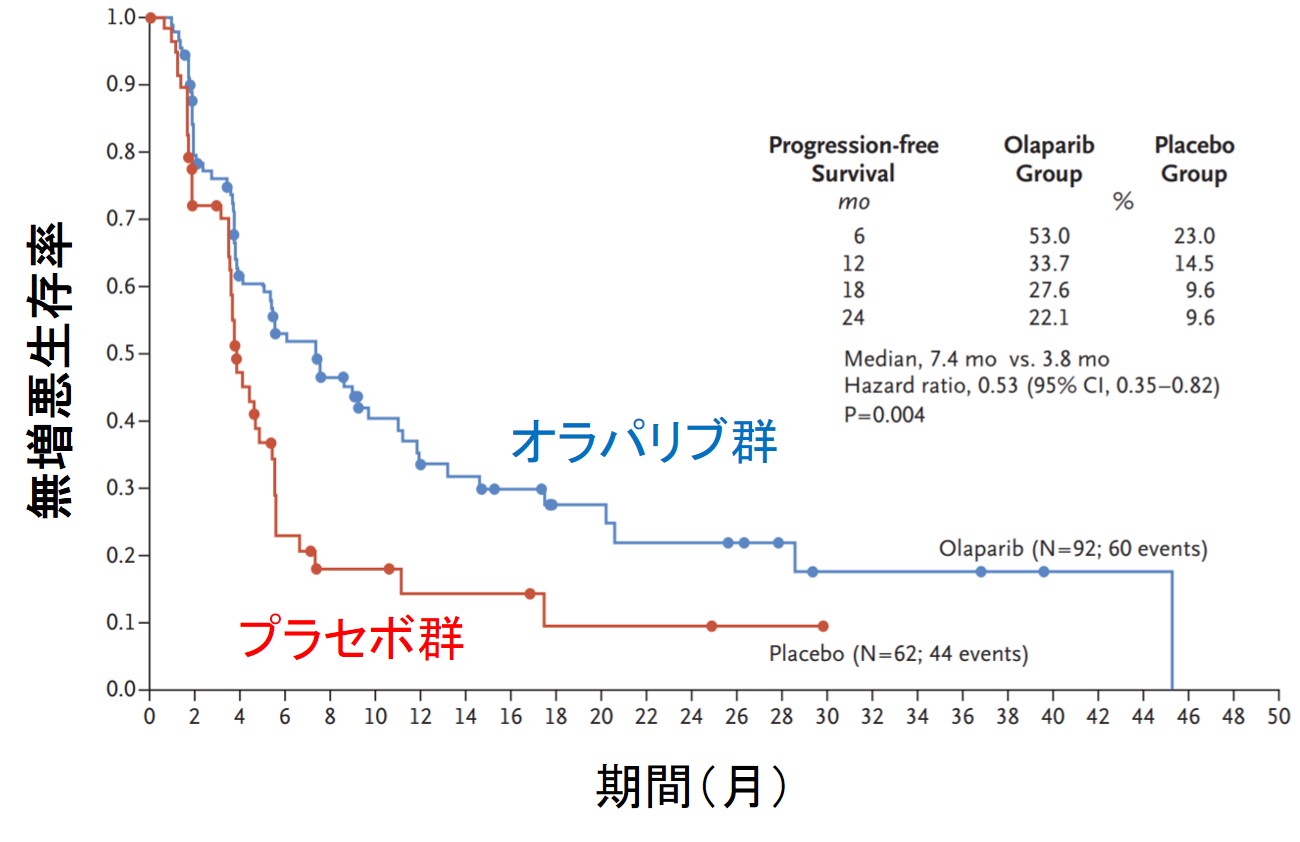
この試験の結果を受け、まずはアメリカ食品医薬品局(Food and Drug Administration)で承認され、その後、(しばらく時間がかかりますが)日本においても安全性・有効性の確認後、承認される流れになると思います。
膵臓がん患者さんの中でBRCA遺伝子変異がある人は比較的少ないのですが、新しい治療の選択肢として期待できます。
国内での状況:膵臓がんに対しては、国内外で未承認。
PEGPH20(ペグ化ヒアルロン酸分解酵素)とゲムシタビン+ナブパクリタキセル併用
膵臓がんでは、組織中に多くのヒアルロン酸が蓄積していることが特徴です。
ヒアルロン酸はがんの悪性度を高めて浸潤・転移を促進し、さらには抗がん剤などの治療が効かない原因になっていることがが明らかとなってきました。
このヒアルロン酸をターゲットとした新しい治療法が、ヒアルロン酸を分解する酵素製剤であるペグ化ヒアルロニダーゼ(PEGPH20)です。
この薬剤によってがん細胞のまわり(間質:かんしつ)のヒアルロン酸をとかし、抗がん剤が届きやすくするという戦略です。
転移性の膵臓がん(ステージ4)に対して、PEGPH20をゲムシタビン(ジェムザール)+ナブパクリタキセル(アブラキサン)と併用することで、無増悪生存率が改善したという第2相ランダム化比較試験(HALO 202)の結果がアメリカから報告されています。
とくにヒアルロン酸が多い膵臓がんに効果が高いという結果でした。
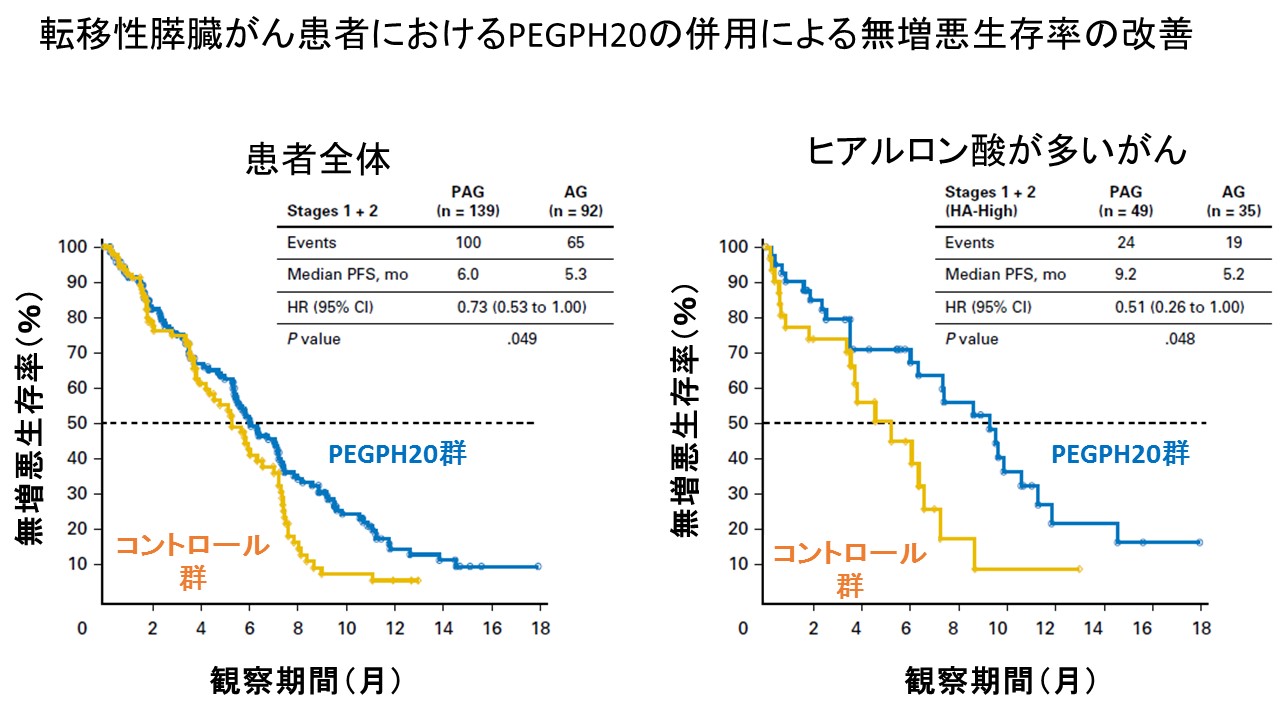
現在、米国で実施されている第3相試験の結果を待ちたいと思います。
国内での状況:国内外で未承認。国外(米国)で第3相試験中
まとめ
膵がんに対して期待できる最新治療を5つ紹介しました。
- 術前補助化学療法(ゲムシタビン+S1)
- キイトルーダ(ペンブロリズマブ)抗PD-1抗体
- S-1+パクリタキセル経静脈・腹腔内投与併用療法
- BRCA変異陽性の膵臓がんに対するオラパリブ(PARP阻害剤)
- PEGPH20(ペグ化ヒアルロン酸分解酵素)とゲムシタビン+ナブパクリタキセル併用
以上です。







20年3月の膵臓がん患者の集いのご講話を楽しみにしていましたが、昨年の台風での中止に続き新型肺炎での中止とは残念です。次回のお話を心よりお待ちしております。
よろしくお願い申し上げます。
コメントありがとうございます。
私自身、みなさんにお会いできるのを楽しみにしておりましたので、大変残念です。
次回こそ実現することを願っております。